抗癌活性を有する“ナノファイバーメッシュ”を作製
温熱療法と化学療法を同時に実現させ上皮性癌細胞の自然死誘導に成功
2013.06.14
独立行政法人物質・材料研究機構
NIMS 国際ナノアーキテクトニクス研究拠点 生体機能材料ユニットの荏原充宏MANA 研究者らは、癌の温熱療法 (ハイパーサーミア) と化学療法 (抗癌剤治療) を同時に実現させることが可能なナノファイバーのメッシュを新たに開発しました。このナノファイバーメッシュを用いることで、上皮性の癌細胞を効率的に自然死 (アポトーシス) させることに成功しました。
概要
- 独立行政法人物質・材料研究機構 (理事長 : 潮田 資勝) 国際ナノアーキテクトニクス研究拠点 (拠点長 : 青野 正和) 生体機能材料ユニット (ユニット長 : 青柳隆夫) の荏原充宏MANA 研究者らは、癌の温熱療法 (ハイパーサーミア) と化学療法 (抗癌剤治療) を同時に実現させることが可能なナノファイバーのメッシュを新たに開発しました。このナノファイバーメッシュを用いることで、上皮性の癌細胞を効率的に自然死 (アポトーシス) させることに成功しました。
- 上皮性の悪性腫瘍のひとつである扁平上皮癌は多くの組織で認められる癌で、例えば、食道癌の90%以上、子宮頚部癌の80%以上、肺癌の30%以上は扁平上皮癌が占めているといわれています。治療方法は、癌の進行度によって手術、放射線療法、化学療法が三本柱となっていますが、これらに加え、近年高い注目を集めているのが温熱療法です。これは癌細胞が正常な細胞と比べ熱に弱いことを利用し、がん細胞を死滅させるものです。しかも温熱療法は、化学療法などと併用することで抗癌剤の効果が向上することがわかっています。しかし、実際に温熱療法と抗癌剤投与を併用するには、独立した2つの治療法を別々に行わなければならず、これまで、同じ場所で同じタイミングで精密に制御することが困難でした。
- 今回の研究では、この問題を克服し、上皮性悪性腫瘍に対して温熱療法と化学療法を同時に行う方法の開発に成功しました。開発したのは患部に直接貼れるメッシュ状の材料で、温度応答性高分子、磁性ナノ粒子、抗癌剤を組み合わせたハイブリッド材料です。これまでも磁性ナノ粒子を用いた磁気温熱療法などが開発されておりますが、磁性ナノ粒子をそのまま体内に投与するため、患部でのハンドリングの難しさや磁性ナノ粒子自体の安全性が懸念されています。本ナノファイバーメッシュはハンドリングしやすく、内視鏡手術などでも使えます。また、ファイバー内の磁性粒子は安定に存在するため体内への拡散も抑えられ、磁性粒子を直接投与する方法と比べて安全性は高いと考えられます。
- このナノファイバーメッシュは、自己発熱体である磁性ナノ粒子を含んでいるため、交流磁場をかけることでファイバーを加熱することができます。そして生じた熱に応答し、温度応答性高分子が収縮することで、内部の抗癌剤を外部に放出させます。ヒトメラノーマ細胞株を用いてこのファイバーの抗癌活性を調べたところ、交流磁場をかけると癌細胞の自然死誘導をON-OFF制御可能であることが明らかとなりました。本開発は、体外からの刺激によってのみ、患部での加熱と薬物放出を同時にON-OFF制御できるため、病気の治療の時空間制御 (任意のタイミング・場所での薬の投与など) が求められている21世紀において、次世代医療材料の開発の大きな前進となると考えられます。
- 本研究成果は、科学雑誌「Advanced Functional Materials」のオンライン速報版で日本時間平成25年6月14日19 : 00 (現地時間14日12 : 00) に公開されます。
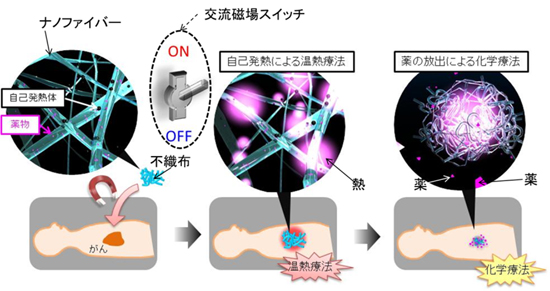
プレス資料中の図1:自己発熱/抗癌剤放出機能を有するナノファイバーメッシュを用いた癌治療
